De quelques formes développées
plus spécialement au XXe siècle
|
Les injections :
(faisaient partie du Groupe 8 de Dupuy) |

Injections, L’Officine de Dorvault, 1855 |
Historiquement, ce terme recouvre des formes d’administration assez diversifiées des médicaments. On l’utilisait en effet pour les médicaments liquides destinés à être introduits à l’aide d’une seringue : il s’agissait donc aussi bien de désigner les injections dans une cavité naturelle ou accidentelles de l’organisme, que les lavements ou encore les injections hypodermiques.
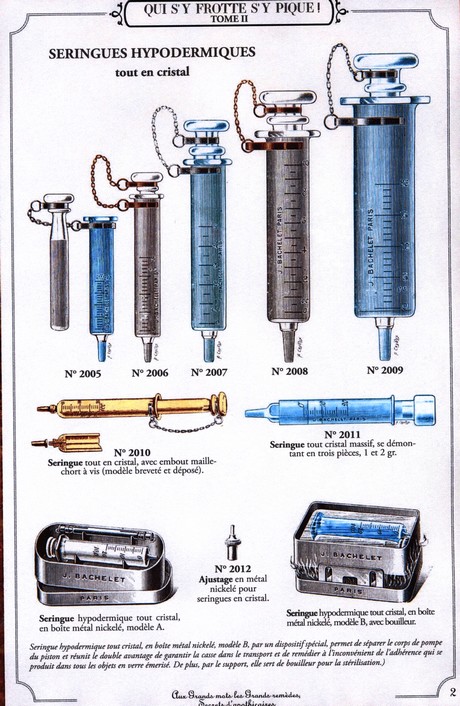
Les seringues furent longtemps de nature très diverses : seringues en verre, en étain à piston ou à poire en caoutchouc, etc. Selon Philippe, médecin au XIXe siècle, c’est Gatinaria (mort en 1496) compatriote de Christophe Colomb, qui fut l’inventeur de la première seringue. Cette invention fut d’abord destinée aux injections à réaliser dans le tube digestif. On utilisait alors le mot grec clystère (signifiant je lave) pour désigner l’injection pour laquelle la seringue avait été inventée. Le mot lavement fut longtemps combattu, en particulier par les jésuites, qui y voyait un usage inapproprié « car ce substantif est employé dans les cérémonies de l’Eglise ». Si bien que Louis XIV ne demanda plus de lavement, mais demanda son remède, et donna l’ordre à l’Académie Française d’insérer ce mot dans son dictionnaire avec l’acception nouvelle.
|
|
Les lavements
Album de galénique pittoresque
Dessin de Jean-Paul Ladril, Editions Pariente, 1996
|
|
La voie parentérale : |
| |
|
|
|
Dans son ouvrage de 1895, Dupuy consacre un chapitre aux injections hypodermiques, dont l’idée, dit-il revient à Fourcroy qui écrivait en 1785 : « Pourquoi n’introduit-on pas, sous la peau des substances actives qui trouveraient là les conditions de l’absorption intégrale et qui détermineraient alors, d’une façon sûre, tous les effets dont elles sont capables ».
En pratique, cette voie d’administration parentérale (voie intraveineuse, voie intra-artérielle, sous-cutanée…) fut peu utilisée jusqu’au XXe siècle en raison des risques infectieux. On réalisait déjà des injections dans la vessie, dans l’urètre, dans le vagin, dans le sac lacrymal. Les débuts médicaux de l’injection intraveineuse se placent au milieu du XVIIe siècle avec Guillaume Harvey (mort en 1657).
On injecta chez l’animal puis peu à peu chez l’homme des liqueurs opiacées ou émétiques (ce fut l’œuvre de Robert Boyle (1657-1664)), puis du vin et de la bière, mais surtout du lait et du sang (J-B. Denis, 1667). Constatant les risques associés à cette technique, un arrêt du Parlement de Paris mit un frein au zèle des novateurs
. |

Les solutions injectables
Album de galénique pittoresque
Dessin de Jean-Paul Ladril, Editions Pariente, 1996 |
L’injection intraveineuse de reparut que vers le milieu du XIXe siècle et resta tenu en suspicion. En 1874, on peut lire dans le Nouveau Dictionnaire de Médecine et de Chirurgie pratiques que l’injection dans les vaisseaux mérite d’être conservée dans la thérapeutique comme dernière ressource dans deux cas : pour lutter contre le choléra (injection de carbonate de sodium) et lorsqu’une perte de sang considérable met le malade en danger de mort immédiate. L’injection hypodermique ou intramusculaire avait encore plus d’obstacle à franchir car les tissus exigent l’asepsie. Lafargue, médecin de St-Emilion dont on fait aujourd’hui l’inventeur de l’hypodermie, se servit de la lancette pour introduire la morphine en pâte sous la peau (1836).
A plusieurs reprises, il a démontré l’intérêt de cette approche. Mais le point de départ de la véritable hypodermie semble bien lié aux travaux de Pravaz et de l’invention de sa seringue (1853). Cette dernière était conçue pour injecter quelques gouttes de liquide et la principale innovation résidait dans l’utilisation d’une aiguille. Charrière, puis Luer, créèrent presque aussitôt d’autres formes de seringues. Le premier propagateur de l’injection hypodermique est sans doute A. Wood, d’Edimbourg, dont les publications sont de 1853-1855. Il utilisait une seringue de type Fergusson. Behier, médecin de l’hôpital Beaujon, à Paris, introduisit la technique de Wood en 1859 : on injectait alors le sulfate d’atropine, le chlorhydrate de morphine et le sulfate de strychnine. Ce n’est véritablement qu’à la fin du XIXe siècle que l’injection parentérale se développe, après la création de l’ampoule par Stanislas Limousin, mais aussi après les travaux sur l’aseptie et les moyens efficaces de stériliser les solutions injectables. Les ampoules délivrées par la Pharmacie Centrale des Hôpitaux de Paris vont passer de quelques centaines en 1916 à plus d’un million par mois dès les années 1950.
|
|
| |
|

Publicité pour l’Endopancrine
Années 1930 |
Les solutés de perfusion, qu’on appelle couramment les solutés massifs, on fait leur apparition en parallèle, et sont nés en 1831 : Thomas Latta avec les Dr Lewins et Craigie, de Leith, traitent trois cholériques par des perfusions de ce qui deviendra le sérum artificiel.
Cette technique sera adaptée par Auguste Philibert Duchaussoy en France, puis par Dujardin-Beaumetz en 1875 et par Georges Hayem qui l’utilisera lors de l’épidémie de choléra de 1884.
A la fin du XIXe siècle, ce type d’injection massive va prendre une place reconnue pour le traitement des hémorragies, puis pour le traitement des maladies infectieuses.
Leur emploi en temps de guerre va stimuler les travaux d’amélioration des solutés massifs.
|
Des solutés de glucose apparaissent à la Pharmacopée en 1926, puis les solutés de bicarbonate dans l’édition de 1937. Les premiers solutés de remplissage sont à base de gélatine, mais également très vite de polyvinylpyrolidone qui sera très employé pendant la seconde guerre mondiale en Allemagne et qui sera commercialisé en France en 1949 sous le nom de Subtosan.
Le dextran, quant à lui, sera commercialisé en France en 1950. Il faudra attendre encore une dizaine d’années supplémentaires pour voir commercialiser les premières émulsions injectables : l’Intralipid, émulsion d’huile de soja, est commercialisée en France en 1965.
|

Ampoules RB
Boite de conditionnement metallique (devant)
XXe siècle |

Ampoules RB
Boite de conditionnement metallique (arrière)
XXe siècle |
C’est le début d’une intense activité de recherche pour mettre au point des mélanges nutritifs de plus en plus complexes.
Après une longue période de contenant en verre pour les solutions injectables, il apparaît en 1971 les premières poches plastiques en polychlorure de vinyle, qui seront suivies quelques années plus tard par les poches de poly-vinyl-acétate puis de polypropylène.
|

Publicités pour les spécialités injectables (Années 1960) |
|
Dans le domaine des formes injectables, la recherche galénique s’est aussi orientée au XXe siècle vers la mise au point de produits vectorisés. Les chercheurs se sont en effet appliqués à mettre au point des systèmes particulaires, submicroniques, pour le transport des médicaments, systèmes permettant à la fois de protéger la molécule active de la dégradation, et d’en contrôler la libération dans le temps et dans l’espace. Dès le début du XXe siècle, Paul Ehrlich rêvait déjà de « magic bullet » susceptible d’acheminer un médicament de manière spécifique vers son site d’action. Son rêve se réalisera en partie avec l’avènement de ce que les anglo-saxons appelèrent les Drug Delivery Systems (DDS). Une société américaine, Alza Corporation, fondée en 1968, fera figure de pionnier dans le développement de ces formes. Bien que pouvant être utilisés par d’autres voies d’administration, c’est principalement par voie intraveineuse que ces nouvelles formes galéniques sont données au patient : liposomes, microsphères, nanoparticules, nanosphères. Après administration intravasculaire, les vecteurs particulaires sont opsonisés, c’est-à-dire recouverts de protéines et reconnus par les macrophages du foie et de la rate. Les chercheurs ont également développés des systèmes particulaires « furtifs » qui, à l’inverse des précédents sont capables de séjourner plus longtemps dans la circulation en évitant la reconnaissance par le foie et la rate. Bien que leur histoire soit encore récente, nous pouvons en retracer quelques éléments essentiels.
|

Publicité pour Leucoseptyl
Laboratoire de l’Endopancrine
Années 1930
|
|
|
|
Les liposomes :
(les illustrations proviennent du moteur de recherche google) |
| |
|
|
Les liposomes sont des systèmes colloïdaux vésiculaires, biocompatibles et biodégradables, composés d’une ou de plusieurs bicouches de phospholipides organisés en phase lamellaire, et délimitant un ou plusieurs compartiments aqueux.
L’histoire des liposomes peut être considérée comme issue de la découverte, en biologie cellulaire, de la structure en bicouche des membranes des cellules.
|
Les travaux de Dervichian, Luzzati, Chapman et d’autres ont conduit à préparer des modèles de biomembranes artificielles sous la forme de liposomes qui se sont avérés capables d’encapsuler et de relarguer des ions, comme l’a montré Bangham en 1965.
Dans les années 1970, Gregoriadis et Ryman ont eut l’idée les premiers d’utiliser les liposomes comme vecteurs de médicaments.
|
|
|
|
D’autres comme Demetrios Papahadjopoulos ont fortement contribué à faire évoluer les connaissances dans ce domaine. Ce dernier, qui avait été dans le laboratoire de Bangham en 1966, fut ensuite en charge de recherche au Roswel Park Memorial Institute de Buffalo, dans l’Etat de New York, de la mise au point de méthodes reproductible de production des liposomes. De très nombreux travaux ont été réalisés depuis plus de 20 ans sur cette forme galénique originale, et plusieurs sociétés pharmaceutiques ont fondés des grands espoirs sur elle pour diriger les médicaments vers des cibles biologiques précises et comme adjuvant des vaccins.
|
|
Au début des années 1980, plusieurs équipes de recherche vont s’intéresser à l’incorporation d’Amphotéricine B dans les liposomes. En 1981, New et son équipe étudièrent l’activité anti-leshmaniale de ce médicament et d’autres antifongiques sous la forme de liposomes. Quelques mois plus tard, Graybill publia ses travaux sur le traitement de la souris infectés par Cryptococcus neoformans grâce à cette nouvelle forme. Les auteurs concluaient que la plus faible toxicité du médicament sous cette forme permettrait de donner des doses nettement plus élevées.
|
|
|
|
Ces résultats furent confirmés chez l’homme quelques années plus tard, donnant naissance au premier produit injectable commercialisé en Europe sous cette forme, l’AmBisome®, dans les années 1990 (en 1998 en France). Ce médicament, présentée sous forme de lyophilisat et réservé à l’usage hospitalier, est indiqué dans certaines mycoses.
Deux autres médicaments ont également été mis sur le marché sous cette forme : le Myocet®, complexe de citrate de doxorubicine encapsulé dans des liposomes, destiné au traitement du cancer du sein ; et le Caelyx®, approuvé par l’Union européenne en 1996, chlorhydrate de doxorubicine sous forme de liposomes, pour le traitement de plusieurs types de cancer.
|
| |
|
Entre les travaux initiaux des précurseurs comme Bangham et Gregoriadis et la mise sur le marché des premiers produits, le cheminement de la recherche s’est révélé extrêmement complexe pour aboutir à cette forme pharmaceutique qui reste marginale aujourd’hui dans l’arsenal des formes galéniques possibles.
Les premières années de recherche dans les années 1970 permirent de montrer l’interaction des liposomes avec les systèmes biologiques, en particulier les modifications de la pharmacocinétique de ces produits en fonction de leur taille et de la charge électrique des particules, mais aussi la fuite du médicament hors des liposomes et la captation de ces derniers par les macrophages. Fut également découvert dans les années 1970 les propriétés immuno-adjuvantes des liposomes, ouvrant la voix à des recherches active dans le domaine des vaccins.
|
|
|
Pour essayer d’augmenter la quantité de médicament incluse dans les liposomes (quantité initialement très faible), limiter la fuite de substance active et prolonger leur circulation dans le sang, différentes modifications structurales ont été apportées : l’ajout de cholestérol dans la bicouche et le choix de nouveaux phospholipides. A la fin des années 1980, des chercheurs comme Papahadjopoulos eurent l’idée de modifier le taux relatif de substance active et de lipides. Après une forte période d’incertitude, l’industrie pharmaceutique commença à s’intéresser à cette nouvelle forme et à investir pour faire progresser le développement de plusieurs médicaments utilisant les liposomes, dont plusieurs sont sur le marché depuis la fin des années 1990.
|
|
|
|
En parallèle à cette recherche sur les liposomes injectables, des travaux ont été réalisées dans les années 1980 sur l’usage de cette forme pharmaceutique pour l’administration sur la peau.
La première publication sur l’efficacité des liposomes comme vecteur cutané de médicaments date des années 1980 avec les travaux de Mezei et Gulasekharam, ce qui sera de début d’intenses discussions sur l’efficacité des liposomes comme vecteurs transdermique des substances actives.
|
A la fin des années 1990, une nouvelle catégorie de produit de cette classe, fortement déformable, a été mise au point par Cevc et Blume sous le nom de Transdermose®, avec une efficacité considérée par certains chercheurs comme comparable à l’usage de la voie sous-cutanée.
Plus récemment, une autre forme de vecteur lipidique a été mise au point : les ethosomes, riches en alcool, développés par Touitou et son équipe de recherche (1997). L’éthanol confère en effet une forte charge négative en surface des liposomes, réduisant ainsi la taille des particules.
Des produits destinés à cette voie d’administration sont encore aujourd’hui en cours d’évaluation chez l’homme.
|
|
Les nanosphères, microsphères et nanoparticules :
(les illustrations proviennent du moteur de recherche google) |
| |
|
|
|
Suivant l’exemple des liposomes, qui ont l’inconvénient majeur d’être peu adaptés aux molécules lipophiles, d’autres recherches ont été entreprises sur de nouveaux systèmes particulaires.
L’expérience a été concluante : plusieurs produits ont obtenus une autorisation de mise sur le marché en Europe dans les années 1990 et 2000, comme les nanoparticules de polymères (Copaxone®) ou sous forme de suspension (PegIntron®, Somavert®).
Des produits de contraste pour l’échographie sont des particules colloidales (Sonovue®) et pour l’Imagerie de résonance magnétique (IRM), des nanoparticules d’oxyde de fer (Endorem®, Resovist®).
. |
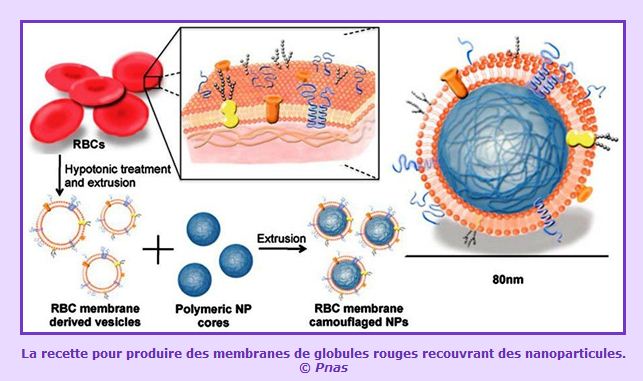 |
Par ailleurs, comme pour les liposomes, plusieurs équipes de recherche ont eu pour objectif d’encapsuler des substances actives, puis si possible de fixer sur les systèmes particulaires des anticorps monoclonaux ou d’autres molécules biologiques susceptibles de modifier radicalement le devenir des produits dans l’organisme en les dirigeant vers des cibles précises. Ce couplage entre une surface de particule et une molécule biologique est une opération complexe qui peut modifier considérablement le comportement de la molécule biologique dans l’organisme
|
|
On voit donc que les recherches menées depuis la fin des années 1940 à l’interface de la physique, de la chimie, et de la biologie ont abouti à la conception, au développement et à la commercialisation de systèmes galéniques originaux, submicroniques, pour des applications diagnostiques et thérapeutiques, plus spécialement dans le domaine de la cancérologie.
. |
|
|
|